Questionnement - Analyse de la réaction
Question⚓
Rappel des données et questions de la fiche
Équation bilan de la réaction :
\(\large{2MnO_{4(aq)}^- + 5 C_2 H_2 O_{4(aq)} + 6H^+_{(aq)} \longrightarrow 10 CO_{2(g)}+2Mn^{2+}_{(aq)} + 8 H_2 O_{(l)}}\)
Constitution du système chimique :
\(V_1 = 10{,}0\ \mathrm{mL}\) de solution de permanganate de potassium de concentration apportée \(C_1=1{,}00\times 10^{-3}\ \mathrm{mol\cdot L^{-1}}\) ;
\(V_2=10{,}0\ \mathrm{mL}\) de solution d'acide oxalique de concentration apportée \(C_2=1{,}00\times 10^{-2}\ \mathrm{mol\cdot L^{-1}}\) ;
\(V_3=2{,}0\ \mathrm{mL}\) de solution d'acide sulfurique de concentration \(5{,}0\ \mathrm{mol\cdot L^{-1}}\).
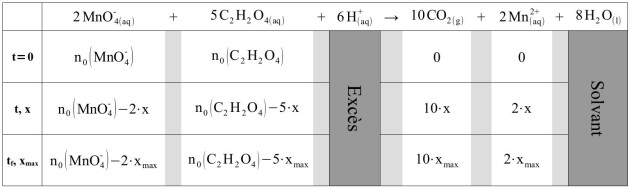
Tableau d'avancement et réactif limitant
Justifier qualitativement que les ions H+ sont en large excès et que la quantité de matière du solvant ne présente pas d’intérêt en termes de suivi.
Complétez le tableau d’avancement de la réaction.
Déterminer le réactif limitant de cette réaction ainsi que la valeur de l’avancement maximal xmax.
Suivi de la réaction au cours du temps
Quelle grandeur physique pourrait être facilement mesurée dans le cas présent et être reliée directement à une quantité de matière ?
Effectuez les calculs et opérations nécessaires pour exprimer l’avancement x en fonction de la grandeur mesurée et de quantités de matières initiales.
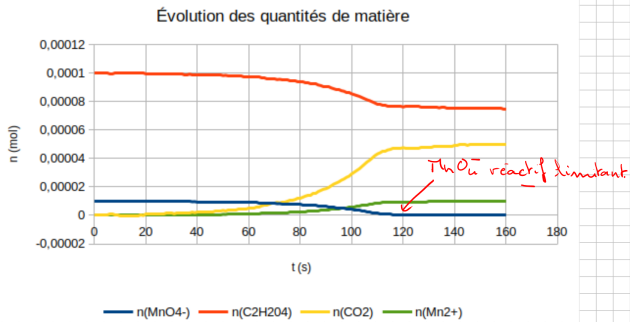
À partir des données brutes de mesures mises à votre disposition, tracez les représentations graphiques de x, \(n\left(MnO_4^-\right)\), \(n\left(C_2H_2O_4\right)\), \(n\left(Mn^{2+}\right)\) et \(n\left(CO_2 \right)\).
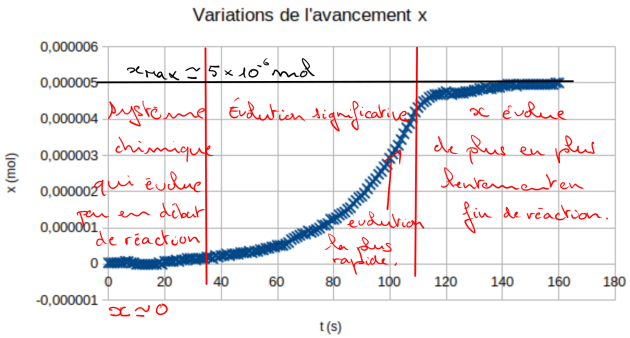
Commenter l’allure des variations de l’avancement x au cours du temps.
Les variations des quantités de matière des réactifs et produits sont-elles en accord avec la valeur de l’avancement maximal et le réactif limitant.
Solution⚓
Tableau d'avancement et réactif limitant
L'acide sulfurique est 500 fois plus concentré que l'acide oxalique et 5000 fois plus concentré que la solution de permanganate. Pour des volumes introduits comparables, on peut donc considérer que les ions H+ sont en très large excès.
Tableau d'avancement complété
Tableau d'avancement de la réaction entre l'acide oxalique et les ions permanganate Pour déterminer le réactif limitant, on compare les valeurs de \(\dfrac{n_0\left(MnO_4^- \right)}{2}\) et \(\dfrac{n_0\left(C_2 H_2 O_4\right)}{5}\)
\(n_0\left(MnO_4^- \right)=1{,}0 \times 10^{-5}\ \mathrm {mol}\)
\(n_0\left(C_2 H_2 O_4\right)=1{,}0\times 10^{-4}\ \mathrm{mol}\)
donc \(dfrac{n_0\left(MnO_4^- \right)}{2}=5{,}0\times 10^{-6}\ \mathrm{mol}\) et \(\dfrac{n_0\left(C_2 H_2 O_4\right)}{5}=2{,}0\times 10^{-5}\ \mathrm{mol}\).
\(\dfrac{n_0\left(MnO_4^- \right)}{2}<\dfrac{n_0\left(C_2 H_2 O_4\right)}{5}\) donc :
\(MnO_4^-\) est le réactif limitant ;
\(x_{max}=5{,}0\times 10^{-6}\ \mathrm{mol}\).
Suivi de la réaction au cours du temps
En présence d'une espèce chimique colorée, on peut envisager une mesure d'absorbance.
D'après la loi de Beer-Lambert, on a \(A=k\cdot\left[MnO_4^-\right]\)
D'après le tableau d'avancement de la réaction :
\(n\left(MnO_4^-\right)=n_0\left(MnO_4^-\right)-2x\)
Par définition, la concentration s'exprime en fonction de la quantité de matière par \(\left[MnO_4^-\right]=\dfrac{n\left(MnO_4^-\right)}{V_{total}}\)
La relation de Beer-Lambert permet d'écrire :
\(A=k \times \left[MnO_4^- \right]=k\times \dfrac{n\left(MnO_4^-\right)}{V_{total}}\)
k est connu et vaut \(\mathbf{1500\ \mathrm{L \cdot mol^{-1}}}\).
Soit : \(A=\dfrac{k}{V_{total}}\times \left( n_0\left(MnO_4^- \right) - 2\times x\right)\)
On peut alors isoler x pour obtenir l'expression suivante :
\(x=\dfrac{n_0\left(MnO_4^- \right)}{2}-\dfrac{A \times V_{total}}{2\times k}\)
4. et 5.
Cliquer sur ce lien pour télécharger la feuille de calcul complétée.
Évolution de l'avancement au cours du temps | Informations[*] Évolution des quantités de matière au cours du temps | Informations[*]