Détermination de la concentration du jus de citron en vitamine C⚓
Rappel : Données du titrage
On presse plusieurs citrons afin d'en extraire le jus qui est ensuite filtré pour le débarrasser de la pulpe.
On cherche à déterminer la concentration en vitamine C de ce jus de citron fraîchement pressé.
On note CVitC la concentration molaire en acide ascorbique (vitamine C) dans le jus de citron : inconnue.
Le réactif titrant est le diiode \(I_{2(aq)}\) dont la concentration molaire dans la solution titrante est \(C_{I_2} = 2{,}50\times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\).
Prise d'essai : volume de jus de citron prélevé à la pipette jaugée pour le titrage : \(V_\text{titré} = 10{,}0\ \mathrm{mL}\).
Couple oxydant/réducteur du diiode : \(I_{2(aq)}/I^-_{(aq)}\).
Couple oxydant/réducteur de l'acide ascorbique (vitamine C) : \(C_6 H_6 O_{6(aq)}/\underbrace{C_6 H_8 O_{6(aq)}}_{Acide\ ascorbique}\).
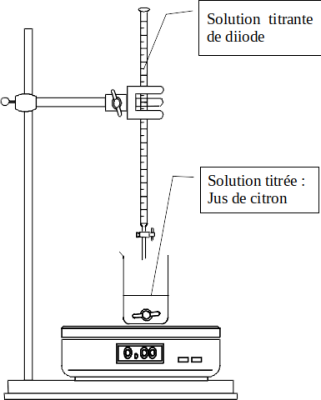
Réaction support du titrage et montage
On titre un volume \(V_\text{titré} = 10{,}0\ \mathrm{mL}\) de jus de citron par une solution de diiode.
La réaction chimique support du titrage est une réaction d'oxydoréduction entre le diiode et l'acide ascorbique. On obtient l'équation de la réaction à partir des demi-équations de chaque couple qui s'écrivent en suivant la méthode vue dans le chapitre Oxydoréduction.
Pour le diiode :
\(I_{2(aq)} \rightarrow I^-_{(aq)}\)
On équilibre l'élément chimique iode :
\(I_{2(aq)} \rightarrow 2I^-_{(aq)}\)
Il reste à équilibrer la charge électrique :
\(I_{2(aq)} + 2e^-\rightarrow 2I^-_{(aq)}\)
Pour l'acide ascorbique :
\(C_6 H_8 O_{6(aq)} \rightarrow C_6 H_6 O_{6(aq)}\)
On équilibre l'élément hydrogène avec des ions \(H^+_{(aq)}\) :
\(C_6 H_8 O_{6(aq)} \rightarrow C_6 H_6 O_{6(aq)} + 2H^+_{(aq)}\)
Il reste à équilibrer la charge électrique :
\(C_6 H_8 O_{6(aq)} \rightarrow C_6 H_6 O_{6(aq)} + 2H^+_{(aq)} + 2e^-\)
L'équation de la réaction support du titrage s'obtient en combinant les demi-équations de façon à mettre en jeu le même nombre d'électrons dans l'oxydation et dans la réduction :
\(\Large{I_{2(aq)} + C_6 H_8 O_{6(aq)} \rightarrow 2I^-_{(aq)}+C_6H_6O_{6(aq)} + 2H^+_{(aq)}}\)
Repérage de l'équivalence et exploitation
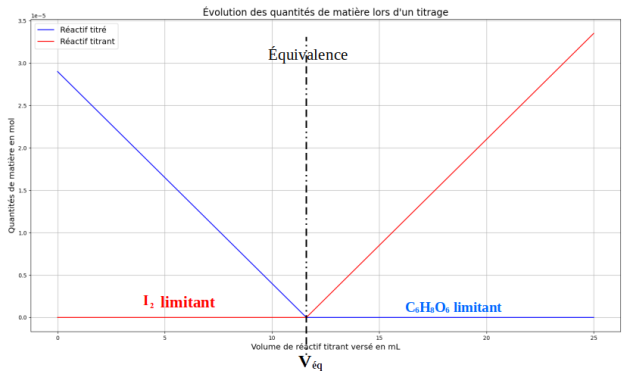
Avant l'équivalence, le diiode est le réactif limitant, il est consommé au fur et à mesure de son introduction dans le système et ne persiste pas dans la solution. Après l'équivalence, il reste en solution.
On met en évidence sa présence en ajoutant dans le système chimique de l'empois d'amidon qui joue le rôle d'indicateur coloré : il prend une teinte noire en présence de diiode.
L'équivalence est repérée par la persistance de la teinte noire dans le bécher.
À l'équivalence, les réactifs ont été introduits dans les proportions stoechiométriques, soit :
\(n_{I_2} = n_{VitC}\)
En faisant intervenir les données du titrage, on peut écrire :
\(C_{I_2} \times V_{eq} = C_{VitC}\times V_\text{titré}\)
On exprime alors la concentration inconnue :
\(C_{VitC} = \dfrac{C_{I_2} \times V_{eq}}{V_\text{titré}}\)
Ci-dessous des exemples de résultats, pour des citrons bio et non bio.
Citrons Bio | Citrons ordinaires |
|---|---|
11,00 | 9,50 |
8,15 | 10,15 |
9,50 | 10,25 |
11,60 | 10,60 |
11,00 |
On prend l'exemple d'un résultat obtenu par un groupe : \(V_{eq} = 11{,}60\ \mathrm{mL}\)
Application numérique :
\(C_{VitC} = \dfrac{2{,}50\times 10^{-3} \times 11{,}60}{10{,}0}\simeq 2{,}90\times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\)
La concentration molaire du jus de citron en vitamine C est donc \(C\left(Vit\ C\right)\simeq 2{,}90\times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\).
Remarque : le nombre de chiffres significatifs pertinent pour l'écriture du résultat sera justifié après la détermination de l'incertitude sur cette valeur.
Complément : Comparaison avec les données nutritionnelles
D'après les données nutritionnelles, un jus de citron contient entre 50 et 60 mg de vitamine C pour 100 mL, soit un titre massique en vitamine C \(t_{VitC}\) compris entre 500 et 600 \(\mathrm{mg\cdot L^{-1}}\).
Le titre massique déterminé par le titrage du jus de citron est :
\(t_{VitC} = C_{VitC}\times M_{C_6H_8O_6}\),
soit \(t_{VitC} = 2{,}90\times 10^{-3}\times 176{,}1\simeq 511\ \mathrm{mg\cdot L^{-1}}\)
Le jus de citron titré dans cet exemple a donc une teneur en vitamine C située dans la fourchette basse des valeurs nutritionnelles couramment admises.
Là encore, le nombre de chiffres significatifs sera justifié après l'estimation de l'incertitude sur ce titrage.
Estimation de l'incertitude sur la concentration en vitamine C⚓
Objectif
Dans cette partie, on s'intéresse à l'estimation de l'incertitude type sur la valeur de la concentration en vitamine C déterminée lors du titrage.
On prend en compte l'ensemble des incertitudes dues à la verrerie et au protocole, en supposant que les prélèvements et les lectures ont été faites avec la plus grande précision possible par les expérimentateurs.
Méthode : Fiche à compléter
La fiche ci-dessous rappelle les sources d'incertitude à prendre en compte ainsi que les relations mathématiques permettant de les calculer. Ces relations ne sont pas à connaître.
Fiche complétée avec un exemple de résultat
La fiche ci-dessous est complétée avec les valeurs de l'équivalence utilisées plus haut.
Écriture du résultat final
Sans arrondi, concentration molaire en vitamine C s'écrit : \(C_{VitC}=2{,}90 \times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\).
L'incertitude type calculée, arrondie à 1 chiffre significatif, s'écrit : \(u \left(C_{VitC} \right)=2\times 10^{-5}\ \mathrm{mol \cdot L^{-1}}\).
En accord avec la précision du dernier chiffre significatif de l'incertitude, on écrira le résultat final sous la forme : \(C_{VitC}=\left(2{,}90 \times 10^{-3} \pm 2 \times 10^{-5} \right)\ \mathrm{mol \cdot L^{-1}}\).
Écriture de l'incertitude sur la concentration en masse (titre massique)
La concentration en masse assortie de son incertitude, calculée dans la fiche corrigée, conduit à : \(t_{vitC}=\left(511 \pm 3\right)\ \mathrm{mg \cdot L^{-1}}\).
Même en prenant en compte l'incertitude, le citron pris en exemple est dans la fourchette basse de la teneur en vitamine C.
Complément : Pour aller (encore) plus loin... visualiser les incertitudes sur une simulation
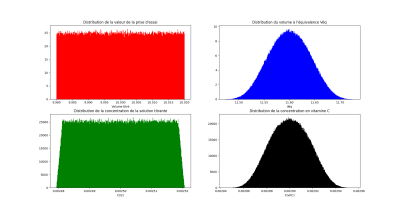
On donne ci-dessous une visualisation graphique des différentes sources d'incertitudes lors de ce titrage : volume titré, concentration de la solution titrante et volume versé à l'équivalence.
Vous remarquez que chaque distribution est centrée sur la valeur que vous avez mesurée ou utilisée dans le TP :
\(V_\text{titré}=10{,}0\ \mathrm{mL}\) ;
\(V_{eq}=11{,}60\ \mathrm{mL}\) ;
\(C_{I_2}=2{,}50\times 10^{-3}\ \mathrm{mol\cdot L^{-1}}\) ;
\(C_{VitC}=2{,}90\times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\).
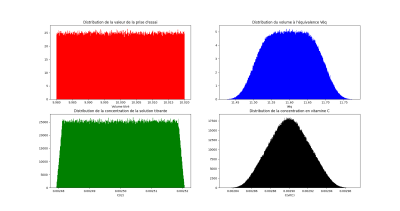
On peut notamment visualiser l'influence de la précision de la détermination du volume à l'équivalence (une ou deux gouttes) sur l'incertitude finale sur la concentration en vitamine C.
Repérage de l'équivalence à une goutte près
Moyenne des valeurs de CvitC : \(\overline{C}_{VitC}\simeq2{,}90\times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\)
Écart-type de la distribution de CvitC : \(\sigma_{n-1}\simeq1{,}68\times 10^{-5}\ \mathrm{mol\cdot L^{-1}}\)
Repérage de l'équivalence à deux gouttes près
Moyenne des valeurs de CvitC : \(\overline{C}_{VitC}\simeq2{,}90\times 10^{-3}\ \mathrm{mol \cdot L^{-1}}\)
Écart-type de la distribution de CvitC : \(\sigma_{n-1}\simeq2{,}09\times 10^{-5}\ \mathrm{mol\cdot L^{-1}}\)
La prise en compte de deux gouttes au lieu d'une sur la détermination de l'équivalence a une influence notable sur la distribution du volume à l'équivalence (forme et largeur) mais finalement peut de répercussion sur la valeur de l'incertitude type si on l'arrondit finalement à un seul chiffre significatif.
Simulation de l'évolution des quantités de matière au cours du titrage⚓
Ci-dessous, la représentation de l'évolution des quantités de matière des réactifs titrant et titré en fonction du volume de réactif titrant versé avec matérialisation de l'équivalence.