La pile à combustible - Une solution d'avenir ?
Question⚓
Cliquez sur le lien ci-dessous pour accéder à l'activité du livre.
Solution⚓
D'après le document 1, on indique que le dihydrogène gazeux à l’anode se transforme en ions hydrogène \(\mathrm{H^+}\).
On a donc la demi-équation suivante : \(\mathrm{H_{2(aq)]} \rightarrow 2H^+_{(aq)}+2e^-}\).
On indique ensuite qu’à la cathode le dioxygène se transforme en eau en réagissant avec ces ions \(\mathrm{H^+}\).
On a donc la demi-équation suivante : \(\mathrm{O_{2(aq)}+4H^+_{(aq)}+4e^- \rightarrow 2H_2 O_{(l)}}\).
À l’anode, la demi-équation traduit une libération d’électrons (ou une perte d’électrons), donc il s’agit
d’une OXYDATION.
À la cathode, la demi-équation traduit une consommation (capture d’électrons), donc il s’agit d’une
RÉDUCTION.
La demi-équation traduisant une libération d’électrons est l’oxydation, donc les électrons partent de l’anode. Ils sont consommés lors de la réduction, donc à la cathode.
Les électrons circulent de l’anode vers la cathode, donc le courant électrique circule de la cathode vers l’anode. L’électrode positive est la cathode.
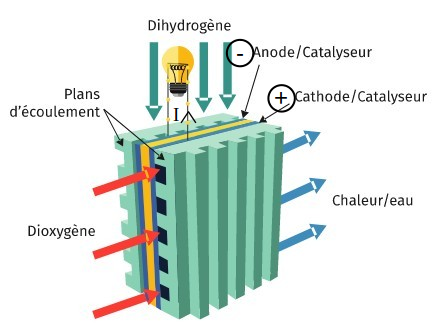
Polarité et sens de circulation du courant dans la pile à combustible | Informations[*] Dans ce type de dispositif, les électrons sont contraints de circuler à l’extérieur de la pile, dans le circuit électrique, au lien d’être échangés directement entre les réactifs. La circulation d’électrons génère un courant électrique dont l’intensité est suffisante pour allumer la lampe.
Le courant électrique circule toujours dans le même sens, donc il s’agit DE COURANT CONTINU.
En combinant les deux demi-équations se produisant aux électrodes, on peut établir l’équation de la réaction chimique globale traduisant le fonctionnement de la pile : \(\mathrm{2H_{2(g)}+O_{2(g)} \rightarrow 2H_2 O_{(l)}}\)
On constate ainsi que le produit de la réaction est de l’eau. En fonctionnement, il n’y a donc aucune émission d’espèce chimique polluante.
Remarque : dans un bilan environnemental complet pour la pile à combustible, il est nécessaire de prendre en compte le mode de production du dihydrogène qui peut présenter une partie polluante.
Synthèse
Cette expérience met en évidence l’exploitation possible d’une grande catégorie de réactions chimiques : les réactions D’OXYDORÉDUCTION.
Elles se caractérisent par UN ÉCHANGE D'ÉLECTRONS entre un RÉDUCTEUR qui LIBÈRE des électrons CAPTÉS par un OXYDANT. Cet échange peut se faire au contact de ces deux espèces chimiques, mais il est possible de faire en sorte que les électrons circulent à travers un circuit fermé pour aller du réducteur à l’oxydant. Dans ce cas, on crée un courant électrique susceptible d’alimenter un circuit constitué d’une lampe comme dans l’exemple du document 1 ou d’un moteur dans le cas d’un véhicule.