Introduction
L'exploitation quantitative des réactions chimiques fait appel à la quantité de matière, exprimée en moles, des espèces chimiques entrant dans la composition du système.
Il n'existe pas d'appareil de mesure permettant d'accéder directement et de manière universelle à la quantité de matière d'une espèce chimique dans un système. Il est donc essentiel de pouvoir relier une grandeur physique mesurable (masse, pression, volume, absorbance, pH, etc...) à une quantité de matière.
Cette activité présente quelques relations indispensables à la résolution de problèmes en chimie.
Quantité de matière⚓
Définition : Quantité de matière
En chimie, la quantité de matière d'une entité est le nombre de moles, noté n, de cette entité.
Elle est notée de la façon suivante : \(n \left(SO_4 ^{2-} \right)=0{,}032\ \mathrm {mol}\), ce qui signifie littéralement « La quantité de matière en ions \(SO_4 ^{2-}\) vaut 0,032 moles. »
Définition : Nombre d'Avogadro
Le nombre d'Avogadro, noté \(\cal N_A\), correspond au nombre d'entités présents dans une mole.
Par définition, \({\cal{N_A}}\simeq 6{,}022\times 10^{23}\ \mathrm{mol^{-1}}\).

Méthode : Relier nombre d'entités chimiques et quantité de matière
La quantité de matière n, exprimée en moles, est liée au nombre d'entités N par la relation :
\(n=\dfrac{N}{\cal {N_A}}\)
Masse volumique⚓
Définition : Masse volumique d'un corps
La masse volumique d'un corps est définie comme le rapport de sa masse sur le volume qu'il occupe.
La masse volumique s'exprime dans le système international d'unités en \(\mathrm{kg \cdot m^{-3}}\).
Elle est cependant couramment exprimée en \(\mathrm{g \cdot mL^{-1}}\) ou encore en \(\mathrm{kg \cdot L^{-1}}\).
Densité et masse volumique⚓
Définition : Densité
La densité est un nombre sans unité correspondant au rapport entre la masse volumique \(\rho\) du corps sur une masse volumique de référence \(\rho_0\).
Dans le cas des liquides et des solides, la masse volumique de référence est généralement celle de l'eau : \(\rho_0 \simeq 1{,}0\ \mathrm{kg \cdot L^{-1}} \simeq 1{,}0\ \mathrm{g\cdot mL^{-1}}\).
Méthode : Interprétation d'une information de densité
La donnée de la densité d s'interprète directement comme une information de masse volumique. Compte tenu de la valeur simple de la masse volumique de référence utilisée, la conversion est aisée.
Par exemple \(d=1{,}23\) s'interprète immédiatement par \(\rho = 1{,}23\ \mathbf{kg\cdot L^{-1}}=1{,}23\ \mathbf{kg\cdot L^{-1}}\).
Concentration massique⚓
Définition : Concentration massique
On définit la concentration massique d'un soluté en solution comme le rapport de la masse m de soluté dissous sur le volume V de solution.
Remarque sur la notation
La concentration massique est parfois notée avec la lettre grecque \(\gamma\).
Pourcentage massique⚓
Définition : Pourcentage massique
Le pourcentage massique d'une espèce chimique X dans un mélange traduit la proportion en masse de cette espèce chimique dans le mélange et s'exprime par la relation ci-dessous.
Quantité de matière d'un gaz - Volume molaire⚓
Définition : Volume molaire
Le volume molaire, noté Vm et exprimé en \(\mathrm{L \cdot mol^{-1}}\), est le volume occupé par une mole de gaz.
Il ne dépend pas du gaz considéré mais dépend de la température et de la pression.
On donne ci-contre quelques valeurs à pression ordinaire.
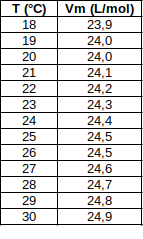
La quantité de matière d'un gaz s'exprime en fonction de son volume et du volume molaire par la relation :